La Impresora de órganos
Ficciones y realidades de la producción de
tejidos artificiales
Gotas con
miles de células, en lugar de tinta, caen de los cabezales sobre una superficie
gelatinosa. Como las gotas que formaban al exterminador de la famosa Terminador,
las células se asocian y arman una estructura en tres dimensiones. A diferencia
del protagonista de ciencia ficción, la bio-impresora fue diseñada para
intentar salvar la vida de millones de personas. Sin embargo, los especialistas
advierten que la ilusión de producir un órgano está aún lejos de
concretarse.
Palabras
claves: ingeniería de tejidos, células madre, tejidos y órganos artificiales
La “impresora de tejidos”
Injertos
artificiales de piel, cartílago y hueso. Córneas, vejigas y hasta vasos
sanguíneos. La ingeniería de tejidos no deja títere con cabeza. Con la
aspiración de construir órganos y regenerar tejidos, se atreve a combinar la
biología con la arquitectura y la ingeniería. Aquí, una de sus últimas y más
audaces apuestas: una impresora de
chorro de tinta modificada que promete producir cualquier parte de nuestro
cuerpo.
Imaginar
que en lugar de una hoja impresa sale una lámina de piel parecería apropiado sólo
en la mente del director cinematográfico James Cameron, concentrado en dirigir
su próxima película de ciencia ficción. Sin embargo, los trabajos del doctor
Vladimir Mironov, de la Universidad de Carolina del Sur en Estados Unidos,
demuestran que nuestra protagonista ya imprimió sus primeros tejidos.
Imprimir en 3D
Una
tecnología propia de arquitectos e ingenieros, que cumplieron el sueño de
materializar sus diseños directamente desde la computadora. ¿Cómo? Con
impresoras que colocan capa por capa el material deseado en el lugar indicado.
Ahora bien, de maquetas a órganos hay un trecho, pero no lo suficientemente
largo como para evitar que Mironov junto al doctor Gabor
Forgacs de la Universidad de Missouri en Estados Unidos
adapten esta tecnología a la medicina regenerativa y de trasplantes.

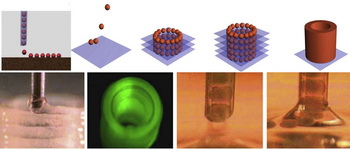
Bioimpresoras.
(Fuente: página web del Dr Mironov, en el
servidor de la Universidad de Medicina de Carolina del Sur, con permiso del
autor http://www.musc.edu/bioprinting/html/how_to_.html ).
“Utilizan
un brazo robótico que, en lugar de tinta, coloca células”, explica el doctor
Pablo Argibay, Director del Instituto de Ciencias Básicas y Medicina
Experimental del Hospital Italiano, y el primero en la Argentina en mantener
con vida a una persona en espera de un trasplante hepático, mediante la
utilización de un xenotrasplante con un hígado de cerdo. Las gotas de bio-tinta
con grupos de miles de células, llamados esferoides, caen en forma precisa y
automática sobre una superficie gelatinosa. Este gel biodegradable, o matriz,
funciona como papel biológico sobre el cual la impresora dirige y coloca cada
gota, según le indique el mapa del órgano en cuestión. Al igual que los
cartuchos de tinta negra y de color, los diferentes tipos celulares necesarios
se colocan en los cabezales. “El robot programado y dirigido por computadora
coloca alternativamente una capa de células y una de matriz”, describe
Argibay.
(Fuente: página web del Dr Mironov, en el
servidor de la Universidad de Medicina de Carolina del Sur, con permiso del
autor http://www.musc.edu/bioprinting/html/how_to_.html ).
Lo más
llamativo de esta técnica, tal vez, sea el uso de una tinta de células. Pensar
en tejidos que se comportan como líquidos es como si en algún punto nos
asemejáramos a aquel exterminador de película. Según el investigador Malcolm
Steinberg de la Universidad de Princeton en Estados Unidos, los tejidos
embrionarios en desarrollo, al estar en suspensión, se redondean y actúan como
gotas. Esas gotas de células agrupadas pueden fusionarse para formar los
órganos y tejidos del embrión. Inspirado en estos trabajos, Mironov diseñó una
tinta de células para la bio-impresora. Utilizó esferoides, que son grupos de
células con una organización similar a la de un tejido, un minitejido.
Precisamente
en la Argentina se hizo algo similar. “En efecto, aquí diseñamos minihígados de
cerdo (esferoides multicelulares y funcionalmente activos), para llenar un
dispositivo externo que podría mantener con vida a un chico en espera del
trasplante por hepatitis fulminante”, detalla Argibay, y aclara: “Cultivamos
células hepáticas de cerdo en condiciones especiales que les permiten crecer
espontáneamente en forma tridimensional. No es una ingeniería tisular guiada,
ni pretende llegar a la complejidad de un órgano”.

La impresora ambiciosa
En su
último trabajo, publicado en la revista Biomaterials a principios de este año,
Mironov plantea la posibilidad de que las gotas de bio-tinta, colocadas lo
suficientemente cerca, se fusionen, pasen de un mini a un macrotejido y así
materializar un órgano.
Mapa para la impresión de un órgano.
(Fuente: página web del Dr Mironov, en el
servidor de la Universidad de Medicina de Carolina del Sur, con permiso del
autor http://www.musc.edu/bioprinting/html/how_to_.html ).
Sin
embargo, Argibay considera que la impresión de tejidos no es el camino a
seguir. “Es una simplificación excesiva. Es reducir el desarrollo de un órgano
a la unión de células y matrices a partir de un diseño, como lo haría un
ingeniero para armar un auto”, remarca. Al contrario, el especialista indica
que un órgano es un conjunto de procesos, señales y conexiones entre las
células que lo conforman. “Jugaría al revés. Partiría de las células, que ellas
crezcan y guíen ese crecimiento, que produzcan su propia matriz”.
El doctor
Juan Carlos Calvo, director del laboratorio de Química de Proteoglicanos y
Matriz Extracelular de la Facultad de Ciencias Exactas y Naturales de la UBA,
afirma: “No es simplemente colocar las células en un orden tridimensional. Se
pueden lograr pequeñas estructuras funcionales, pero hasta el órgano completo
es un salto muy grande”. Por su parte, Argibay declara: “No sabemos dónde
debería ubicarse cada esferoide”. Ambos especialistas coinciden en que la
posición de las células se relaciona con su función. “Hay células cercanas a
los vasos sanguíneos y otras más lejanas, que no hacen exactamente lo mismo.
Las enzimas presentes en cada una varían, porque si estuvieran en la misma,
sería un desastre”, ejemplifica Calvo, experto en tejidos y matriz
extracelular.
La
regeneración de piel es la vedette de la ingeniería de tejidos. Robando cartel
le siguen los injertos de cartílago y hueso. ¿Por qué ellos sí y un riñón no?
Porque son “básicamente sistemas mecánicos”, esclarece Argibay. “Es decir,
armar una capa de tejido con células y matriz es factible. De hecho, se aplica
en la clínica y funciona” afirma el investigador. Incluso, el grupo de Anthony
Atala, de la Universidad de Harvard en Estados Unidos, logró transplantar
vejigas artificiales producidas íntegramente por ingeniería de tejidos. En
cambio, para Argibay, llegar a una estructura que logre dar respuestas complejas
frente a un mar de señales endócrinas, como lo deberían hacer el páncreas y el
hígado, o integrar un compendio de estímulos nerviosos, como lo haría un
corazón, por ahora es más ficción que ciencia.
En este
sentido, la doctora Alejandra Chasseing, directora del laboratorio de
Inmunohematología del Instituto de Biología y Medicina Experimental, previene
sobre la dificultad de lograr que todos los mini tejidos o esferoides sean
funcionales. “Muchos trabajaron en la obtención de células de músculo cardíaco
y no logran hacerlas latir”, ejemplifica la especialista en células madre de
médula ósea.
La impresora se toma revancha
Según
Mironov, las técnicas utilizadas hasta ahora en la producción de tejidos
artificiales, que se basan en hacer crecer células sobre un soporte sólido en
contraposición a la fluidez y fusión de los esferoides, todavía presentan
limitaciones que les impiden llegar a un grado de mayor complejidad.
Los
primeros tejidos impresos en 3D fueron vasos
sanguíneos. Y no por nada. Precisamente, estos conductos son los
encargados de lograr que los nutrientes y, en especial, el oxígeno lleguen a
cada rincón y a cada célula. De hecho, armar una red vascular constituye el
principal desafío de todos los constructores de órganos, que pretenden no sólo
formarlos, sino también que no mueran en el intento. Es allí donde radica la
mayor promesa de la impresión de órganos. Thomas Boland, de la Universidad de
Clemson en Estados Unidos, junto a Mironov logró imprimir estructuras tubulares
ramificadas semejantes a la intrincada red vascular de un órgano.
A
pesar de este auspicioso comienzo, al que se le suman la impresión de parches
de piel y hueso junto con algunos trabajos en tejido nervioso, todavía falta un
largo camino por recorrer. Por su parte, Argibay y Calvo advierten sobre la
visión reduccionista en la que se basa la técnica, por la cual se la condenaría
a no ir más allá de los tejidos simples ya logrados por otras metodologías. A
su vez, mantener la forma e integridad de los órganos en ausencia de un soporte
sólido, obtener una red completa de vasos sanguíneos para irrigar a todo el
tejido y principalmente contar con una producción continúa de esferoides o mini
tejidos son sólo algunos de los temas que desvelan a los impresores de órganos.
¿Cartuchos recargables?
El
obstáculo que se repite en la mayoría de las técnicas de ingeniería de tejidos,
y la impresión de órganos no es la excepción, es obtener la cantidad de células
suficiente para regenerar o, en este caso, imprimir la zona lesionada.
La oferta
no es tan amplia. “Se podrían utilizar las células del mismo tejido a reparar,
como es el caso de pacientes quemados”, explica Argibay, “en los que se realiza
una biopsia y esa muestra se expande en cultivo”. Sin embargo, Calvo señala que
la capacidad de regeneración de la piel, al igual que la de hígado, es poco
común entre los demás tejidos del cuerpo.
Nos
topamos, por consiguiente, con las multifacéticas, controversiales y
definitivamente famosas células madre. También conocidas como progenitoras,
estas células pueden dar origen a los diferentes tejidos y órganos que
conforman nuestro cuerpo. Las hay de embrión o adultas, y cada una lleva
consigo un mundo de expectativas y frustraciones.
“Dejando
de lado todo lo ético, las células madre embrionarias presentan una gran
capacidad de autorrenovación, que permite obtener, de manera rápida, una
importante cantidad de células”, asegura Calvo. Paradójicamente, en esa ventaja
se basa su peligrosidad. “Es factible que generen tumores”, advierte el
investigador. A su vez, en el corazón del dilema ético que engendran, por ser
embrionarias, está su segunda ventaja: pueden dar origen o diferenciarse a
cualquier tejido del cuerpo.
Por otra
parte, la utilización de células madre adultas, si bien exime
a los investigadores de las controversias bioéticas, les generan nuevos
conflictos. A pesar de estar presentes en todos nuestros tejidos,
encontrar esta clase de células puede desesperar a más de uno. Tal es el caso
de las mesenquimales, un tipo de célula madre obtenida a partir de médula ósea.
“De cien mil células mononucleares del mejor donante de médula sólo una es
mesenquimal”, especifica Chasseing. Además de la desalentadora cantidad
conseguida, las células madre adultas no dan origen a todos los tejidos ni se
autorrenuevan tanto como las embrionarias.
El camino
está lejos de llegar a su fin. Lograr que una célula madre, cualquiera sea su
origen, se diferencie a una con características específicas de un determinado
tejido, no es tarea sencilla. “Hay que conseguir el ambiente propicio”, informa
Calvo. En este punto, las células madre adultas corren con ventaja respecto a
las embrionarias. “Ya están encaminadas hacia ese tejido de donde se las
obtuvo”, explica Chasseing.
El último
producto del mercado, con el cual se podría llegar a alimentar nuestra
impresora, pretende dar por tierra el uso de las células madre tal como lo
conocemos hasta ahora. ¿De qué forma? Según los especialistas, con la
introducción de tres o cuatro genes se puede lograr que cualquier célula de
nuestro cuerpo se transforme en madre.
Investigar antes que imprimir
La
trascendencia que implicaría el éxito de la impresión de órganos y las demás
técnicas que sustentan la medicina regenerativa es muy clara. De acuerdo al
pionero en ingeniería de tejidos Robert Langer, del Massachusetts Institute of
Technology en Estados Unidos, 50 millones de personas ya se
beneficiaron gracias a ellas. En el futuro, una de cada 5 personas mayores de
65 años es probable que requiera de estos avances. Las aplicaciones exitosas,
que provocaron los cambios más radicales en los pacientes, incluyen la
recuperación de glóbulos blancos y plaquetas en personas con leucemia, la
disminución del rechazo en los trasplantados, la regeneración de piel en los
quemados y la posibilidad de caminar en los chicos con escaso desarrollo óseo.
Incluso en la Argentina, además del hígado bioartificial diseñado por Argibay y
su grupo, contamos con injertos de piel, cartílago y hueso, y hasta intentos de
córnea fabricados por ingeniería tisular.
Sin
embargo, sería irresponsable y hasta un poco arrogante pasar por alto los
peligros que implican determinadas metodologías. La fantasía terapéutica es el
primero de ellos y, tal vez, el más dañino. Creada por el sensacionalismo de
los mal llamados “avances”, es un atentado a las ilusiones y al estado
emocional del paciente. “La persona se deprime y es probable que se le estén
quitando años de vida”, opina Argibay. A su vez, Chasseing suma algunos riesgos
más: la capacidad de las células madre de producir tumores, de migrar dentro
del cuerpo con la posibilidad de generar metástasis, de diferenciarse a un
tejido inadecuado como los casos de osificación de corazón y hasta de causar
una arritmia por falta de sincronización de las células musculares
cardíacas.
Argibay
concluye: “Hay que saber y después aplicar. Me inclinaría a estudiar la
fisiología de los órganos y a abrir laboratorios que se dediquen a investigar
cómo se forman. A aprender más sobre células madre y medicina regenerativa.
Antes de imprimir tejidos, falta hacer mucha ciencia básica”.
Referencias
Visconti
RP, Kasyanov
V, Gentile
C, Zhang J, Markwald RR, Mironov V. 2010. Towards organ printing: engineering an intra-organ branched
vascular tree.Expert
Opin Biol Ther. 10 :409-20.
Mironov V,
Visconti R, Kasyanov V, Forgacs G, Drake C, Markwald R. 2009. Organ printing:
Tissue spheroids as building blocks. Biomaterials. 30: 2164-74.
Khademhosseini
A, Langer
R. 2007. Microengineered hydrogels for tissue
engineering. Biomaterials 28: 5087-92.
Jakab K, Neagu A, Mironov V, Markwald RR, Forgacs G. 2004. Engineering biological structures of prescribed shape using
self-assembling multicellular systems. Proc
Natl Acad Sci U S A. 101:2864-9.
Jakab K, Neagu A, Mironov V, Forgacs G. 2004. Organ printing: fiction or science. Biorheology. 41: 371-5.
Boland
T, Xu T, Damon B, Cui X. 2006. Application of inkjet printing to tissue engineering. Biotechnol J. 1: 910-7.
Links:
- Página web del Dr Mironov, en el
servidor de la Universidad de Medicina de Carolina del Sur http://www.musc.edu/bioprinting/html/how_to_.html
- Video demostrativo de la impresora de
tejidos.
- Reflexiones
sobre los avances científicos: Artículo publicado en Diario Médico, el 29 de noviembre de 2002, que
mereció el premio nacional "Reflexiones 2002".
Romina P. Carnevale
Doctora en Ciencias Biológicas de la
Facultad de Ciencias Exactas y Naturales de la Universidad de Buenos Aires,
docente universitaria y de nivel medio.
ISSN 1666-7948 www.quimicaviva.qb.fcen.uba.ar |